Potente atividade antiviral in vitro do extrato de Cistus incanus contra o HIV e os Filovírus tem como alvo proteínas do envelope viral
Stephanie Rebenburg, Markus, Martha Schneider, Herwig Koppensteiner, Josef Eberle, Michael Schindler, Lutz Gürtler, Ruth Brack-Werner - Sci Rep . 2016; 6: 20.394. Publicado online em 2 de fevereiro de 2016 doi: 10.1038 / srep20394 - https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4735868/
Helmholtz Zentrum München - Centro Alemão de Pesquisa em Saúde Ambiental, Instituto de Virologia, Oberschleißheim - Centro Alemão de Pesquisa de Infecção, o site associado em Munique, Alemanha.
Sumário
Novas opções terapêuticas são urgentemente necessárias para melhorar o tratamento geral de infecções por vírus. Produtos à base de plantas com características clínicas de segurança correspondentes são um material de partida atraente para a identificação de novas atividades antivirais. Aqui demonstramos que os produtos à base de plantas de Cistus incanus (Ci) inibem in vitro as infecções pelo vírus da imunodeficiência humana (HIV) . O extrato de Ci inibiu os isolados clínicos de HIV-1 e HIV-2 e, acima de tudo, um vírus isolado com resistência múltipla a medicamentos, confirmando extensa atividade anti-HIV. A atividade antiviral foi altamente seletiva para partículas de vírus, evitando a ligação primária do vírus à superfície celular e proteínas do envelope viral de ligação à heparina. O fracionamento guiado por bioensaio indica que o extrato de Ci contém numerosos compostos antivirais e, portanto, tem uma propensão favoravelmente baixa a induzir resistência a vírus. De fato, nenhum vírus resistente emergiu por 24 semanas de propagação contínua de vírus na presença de extratos de CI. Finalmente, o Ci também extrai a infecção inibida por vírus de partículas pseudotipadas com proteínas do envelope do vírus Ebola e Marburg, indicando que a atividade antiviral do extrato de Ci se espalha para patógenos virais emergentes. Atividade antiviral in vitro contra vírus que causam doenças fatais em seres humanos e são fontes promissoras de agentes direcionados a partículas virais.
Neste estudo, investigamos as atividades antivirais de Cistus incanus (Rosa Jara) contra HIV e filovírus. Cistus incanus (Ci) é nativo das regiões mediterrâneas do sul da Europa e norte da África e pertence a uma ordem taxonômica diferente (Malvales) do que Pelargonium beenides (Geraniales). Demonstrou-se que os extratos de Ci têm efeitos anti-inflamatórios, antioxidantes, antifúngicos e antibacterianos 16 , 17 , 18 , 19 . Ci é rico em polifenóis 18 , 19 , 20 , 21 , 22 , 23, Classe química de compostos que inclui muitos representantes com atividades antivirais / antimicrobianas 24 , 25 . Além disso, os extratos de Ci demonstraram inibir a infecção pelo vírus A 21 , 26 . Várias preparações estão disponíveis comercialmente, incluindo decocção CYSTUS052 ® , pastilhas para garganta e chá de ervas. Estudos clínicos conduzidos com pacientes com infecções reveladas do trato respiratório superior diminuíram os sintomas e menos efeitos adversos nos pacientes tratados em comparação aos pacientes controle, indicando a eficácia clínica e o perfil de segurança favorável do CYSTUS052 ® 27 , 28 .
Demonstramos que os extratos de Ci mostram extensa atividade inibitória contra diferentes isolados de HIV, incluindo um vírus clínico isolado com resistência múltipla a medicamentos convencionais. Estudos de modo de ação demonstram que o Ci extrai proteínas alvo no envelope viral, evitando a ligação primária do vírus às células hospedeiras. A atividade antiviral dos extratos de CI também é direcionada contra a proteína do envelope do vírus Ebola. Estudos revelaram que os extratos Ci de extrato de deconvolução contêm numerosos ingredientes ativos contra os vírus HIV e Ebola. Nossos resultados demonstram que o extrato de Ci possui atividade antiviral potente contra os vírus HIV e Ebola e indica que o extrato de Ci contém vários compostos que impedem que esses vírus entrem nas células hospedeiras para replicação.
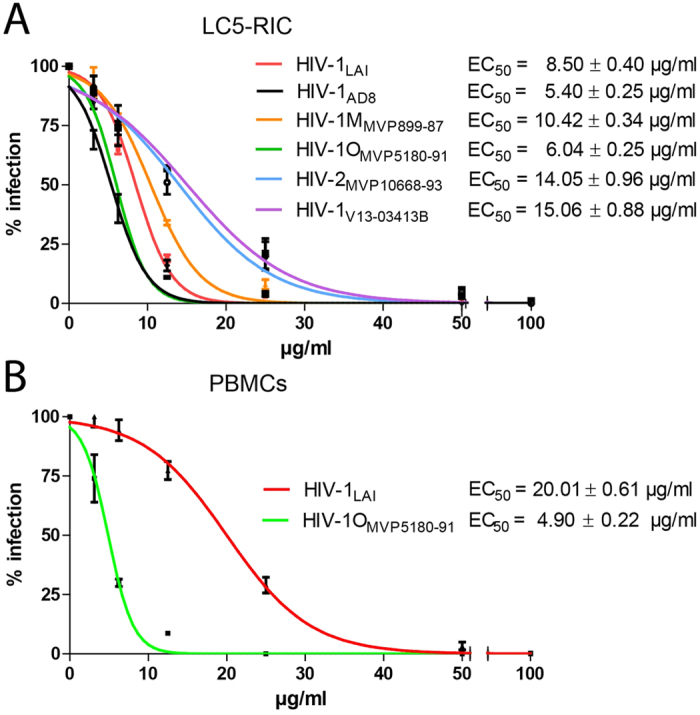
( A ) A atividade antiviral do extrato de Cistus incanus (Ci) inibe os isolados de HIV tipo 1 e 2 do HIV . A inibição da infecção foi avaliada com células Reporter HIV humanas (LC5-RIC ou LC5-RIC-R5 para HIV-1 AD8 (R5) ) usando isolados de HIV-1 com diferentes tropismos de co-receptores ( LAI HIV-1 : X4- trópico; HIV 1 AD8 (R5) : R5-trópico), isolados clínicos de HIV-1 pertencentes ao M (Major) (HIV-1 M MVP899-87 ) ou ao grupo o (outlier) (HIV-1O MVP5180-91 ), um isolado clínico do HIV tipo 2 (HIV-2 MVP10668-93 ) e uma clínica de HIV-1 isolada com resistência a múltiplos medicamentos (HIV-1 V13-03413B ) ( B ) O extrato de Cistus incanus (Ci) inibe a infecção pelo HIV de células-alvo humanas primárias. As células mononucleares do sangue periférico estimuladas pela interleucina-2 (PBMC) foram expostas ao IAF do HIV-1 ou ao MVO de 1O-HIV MVP5180-91 vírus na presença de diferentes concentrações de extrato de Ci. Os níveis de vírus infecciosos produzidos pelo PBMC foram determinados através da análise de sobrenadantes da cultura do PBMC com células LC5-RIC. As experiências foram realizadas com PBMC de 3 doadores. As curvas de dose-resposta são mostradas para 3 ensaios de infecção independentes, cada um realizado com 6 concentrações de extrato de Ci entre 100 g / ml e 3,12 g / ml. Os símbolos significam valores médios e barras de erro, o desvio padrão da média. CE 50 significa a concentração efetiva máxima média calculada.
Cystus052
O extrato Ci comercial padrão do Cystus052 ® foi testado clinicamente, mostra muitas atividades biológicas benéficas para a saúde humana e anteriormente demonstrou inibir a replicação do vírus influenza A na cultura de células 26 e em um modelo animal 21 (consulte também a introdução). Aqui, demonstramos potentes efeitos antivirais do extrato de Ci contra o HIV e o filovírus e demonstramos que os componentes do envelope têm como alvo o extrato de Ci viral, bloqueando a ligação das partículas do vírus às células.
O estudo da atividade anti-HIV do extrato de Ci (extrato total e fração enriquecida em polifenol) com múltiplos isolados de HIV revelou eficácia antiviral comparável contra isolados clínicos que representam diferentes genótipos principais de HIV, incluindo HIV tipo 1 e tipo 2 e Grupo O do HIV-1, bem como o grupo M. Esse achado foi inesperado devido à alta diversidade genética entre os tipos 1 e 2 do HIV (mais de 50% de diversidade de aminoácidos) e o grupo M e O do HIV-1 (diversidade aminoácidos mais de 35%) 45 . Além disso, o grupo O do HIV-2 e HIV-1 é menos suscetível a vários medicamentos anti-HIV aprovados do que o grupo M. do HIV-1. Portanto, o HIV-2 é inerentemente resistente ao T20 (Efavirenz) e ao grupo O do HIV. -1 a vários inibidores da integrase e da transcriptase reversa não-nucleósido 46 , 47 , 48 , 49 . Além disso, o extrato de Ci impedirá a infecção por partículas virais contendo proteínas do envelope de vírus Ebola ou Marburg, demonstrando que a atividade antiviral do extrato de Ci também é direcionada aos componentes do envelope de filovírus. Juntamente com relatórios anteriores da atividade anti-Influenza A 21 , 26 , esses resultados indicam que o extrato de Ci mostra atividade antiviral de amplo espectro contra vários principais patógenos virais humanos não relacionados (por exemplo, HIV, vírus de Marburg) , Vírus Ebola, vírus Influenza A) .
Diferentes ensaios experimentais projetados para investigar o modo antiviral de atividade do extrato de Ci revelaram que o extrato de Ci impede que as partículas do vírus interajam com as células hospedeiras. O tratamento com extrato de Ci bloqueado fornece o RNA viral nas células, demonstrando que o Ci atua no nível de entrada. Os ensaios de tempo de adição indicaram que o tratamento com Ci bloqueou a entrada do vírus em um estágio muito inicial, antes da fusão das membranas viral e celular. Além disso, o tratamento com Ci inibe a ligação de partículas virais marcadas com GFP (HIV-1 e vírus pseudotipado pelo Ebola) às células. Tomados em conjunto, esses resultados confirmam que o tratamento com Ci previne a ligação primária das partículas virais às células, um mecanismo de ação que confere proteção máxima das células hospedeiras contra ataques de vírus. A diferença de,50 , 51 , 52 . A coleção dos medicamentos anti-HIV atuais aprovados clinicamente contém apenas dois inibidores de entrada 3 , ou seja, inibidor de fusão T20 e bloqueador de co-receptores CCR5 Maraviroc. A maioria dos medicamentos aprovados são enzimas alvo do HIV, isto é, protease, transcriptase e alguns inibidores da integrase reversa. Como o extrato de Ci inibe o HIV por uma ação de modo diferente, ele deve ser capaz de inibir vírus com resistência a medicamentos comumente usados. De fato, mostramos que o extrato de Ci efetivamente bloqueou in vitro a replicação de um multi-HIV-1 resistente isolado (HIV-1 V13-03413 ) com mutações que conferem resistência a todos os medicamentos aprovados para protease e inibidor da transcriptase reversa.
Este estudo também fornece evidências de que os componentes antivirais do Ci extraem proteínas do envelope viral e mostram seletividade para mais componentes celulares virais. Os ensaios de pré-incubação confirmaram que os componentes antivirais do extrato de Ci os direcionam especificamente para as partículas virais, mas não são retidos pelas células hospedeiras. Mais apoio à seletividade de vírus da atividade antiviral do extrato de Ci vem dos ensaios de captura de vírus HIV-1 realizados neste estudo, que mostram que o extrato de Ci inibe a gp120 mediada pela ligação de partículas de vírus à heparina, mas não impede a ligação do hospedeiro da célula beta derivada da proteína CD44 ao seu ligante de anticorpo. Bloqueio seletivo de gp120,
Não apenas o HIV-1 33 , mas muitos outros vírus não relacionados usam resíduos proteoglicanos de heparina e sulfato de heparano para ligação primária às células. Além dos filovírus, incluem vírus herpes e hepatite B e vírus C 53 , 54 , 55 , 56 . Nossa descoberta de que o extrato de Ci bloqueia a ligação de componentes virais a detritos celulares usados por vários vírus para fixação fornece ainda suporte para uma extensa atividade de extrato de Ci contra diferentes vírus. Recentemente, também foi relatado que um produto natural de chá verde de molécula única inibe a ligação primária de diferentes virions a heparan sulfato glycans 57, Fornecer evidências do surgimento de um amplo espectro de produtos naturais que bloqueiam a ligação do vírus às células. No que diz respeito ao HIV, o direcionamento da gp120 sugere que o extrato de IC também pode proteger as células das conseqüências nocivas das interações célula-gp120 que vão além da entrada do HIV. Isso inclui a indução de eventos de sinalização aberrantes 58 , 59 , apoptose das células T 60 e dano neuronal 61 , 62 .
Experiências de cultura celular projetadas para investigar a propensão do extrato de Ci para induzir resistência a vírus não revelaram conseqüências do vírus Ci resistente por 24 semanas (= 168 dias) da passagem do HIV-1 na presença de extrato de Ci. Por outro lado, o risco de resistência ao vírus foi relatado como sendo muito maior para o inibidor de ligação única Fostemsavir (BMS-663068) 63 . Portanto, 14 dias de seleção em cultura de células foram suficientes para gerar Fostemsavir resistente ao vírus LAI do HIV-1 e uma única substituição de aminoácidos no LAI do HIV-1 Env foi suficiente para resistência. Estudos de fracionamento guiados por bioensaio indicam a presença de múltiplos compostos antivirais no extrato de Ci. Essa combinação de moléculas ativas é presumivelmente responsável pelo baixo risco de surgimento de vírus resistentes durante o tratamento com Ci, em comparação com o tratamento com drogas antirretrovirais de composto único.
Este estudo demonstra uma atividade antiviral potente e ampla do extrato de Ci em condições de cultura de células. Além disso, estudos clínicos demonstraram um perfil de segurança favorável para o extrato de Ci in vivo 27 , 28 . Embora essas observações apóiem uma exploração adicional das atividades antivirais do extrato de Ci, é importante notar que não defendemos o uso do extrato de Ci como fármacos com base nos resultados apresentados neste estudo. Avaliação do potencial do extrato de Ci para in vivoAplicações terapêuticas antivirais requerem uma extensa pesquisa futura. Um passo importante nessa direção será a identificação de agentes antivirais de extrato individuais e a análise de suas propriedades farmacocinéticas de Ci. Outro caminho para a exploração da aplicação in vivo do extrato de Ci é o seu uso potencial como microbicidas tópicos para impedir a transmissão sexual da transmissão do HIV 64 . A resistência da atividade antiviral a um pH baixo e as altas temperaturas encontradas neste estudo estão incentivando ainda mais as propriedades do extrato de Ci que suportam sua exploração para aplicações tópicas.
Por fim, o extrato de Ci também pode fornecer uma fonte para a mineração de novos agentes antivirais. Portanto, os produtos naturais estão recuperando popularidade pela descoberta de medicamentos devido à superação de várias restrições das bibliotecas sintéticas, incluindo a diversidade química limitada 65 . Além disso, os produtos naturais provaram ter sido muito bem-sucedidos no desenvolvimento de medicamentos no passado, com 34% dos medicamentos aprovados pela FDA 1981-2010 sendo baseados ou derivados de produtos naturais 66. É mostrado que a atividade antiviral pode ser isolada do extrato de Ci por enriquecimento de compostos polifenólicos e é retida ao longo de numerosas etapas de fracionamento seqüencial. Isso indica que agentes ativos com complexidade reduzida podem ser produzidos a partir do extrato de Ci. A identificação de compostos ativos individuais a partir do extrato Ci complexo ou simplificado pode produzir potenciais para novos agentes antivirais, bem como fornecer moléculas de assinatura para monitorar as propriedades farmacológicas dos agentes antivirais derivados de Ci em estudos clínicos. Vá:
Conclusão
O extrato de Ci combina ampla atividade antiviral com baixo risco de resistência a vírus. Seu mecanismo de ação envolve o bloqueio da ligação do vírus às células primárias por direcionamento seletivo das glicoproteínas do envelope viral. Em contraste, muitos outros produtos naturais com componentes da atividade antiviral de amplo espectro da célula hospedeira alvo 67 . Nossos resultados demonstram que vários componentes antivirais no extrato de Ci ligam o vírus à célula hospedeira. No geral, os amplos e poderosos efeitos antivirais in vitro do extrato de Ci demonstrados neste estudo apoiam uma exploração adicional do extrato de Ci e seus componentes para novas abordagens antivirais.

Referências:
- 16. Chinou I., Demetzos C, Harvala C., Roussakis C. & Verbist J. e antibacterianos citotóxicos e diterpenos do tipo labdano das partes aéreas de Cistus subsp incanus. creticus. Planta Medica 60, 34-36 (1994). [ PubMed ] [ Google Acadêmico ]
- 17. Bouamama H., Villard J., Benharref A. e Jana M. Atividades antibacterianas e antifúngicas de Cistus incanus e extratos de folhas de C. monspeliensis. Therapie 54, 731-733 (1998). [ PubMed ] [ Google Acadêmico ]
- 18. Riehle P., Vollmer M. & Rohn S. Compostos fenólicos em infusões de ervas de Cistus incanus - capacidade antioxidante e estabilidade térmica durante o processo de fermentação. Food Research International 53, 891-899 (2013). [ Google Acadêmico ]
- 19. Wittpahl G. et al. Composição polifenólica do chá de ervas de Cistus incanus e sua atividade antibacteriana e antiaderente contra Streptococcus mutans. Medica Planta (2015). [ PubMed ] [ Google Acadêmico ]
- 20. Petereit F., Kolodziej H. & Nahrstedt A. flavan-3-oles e proantocianidinas de Cistus incanus. Phytochemistry 30, 981-985 (1991). [ Google Acadêmico ]
- 21. Droebner K., Ehrhardt C., Poetter A., Ludwig S. e Planz O. CYSTUS052, um extrato vegetal rico em polifenóis, exerce atividade de vírus anti-influenza em camundongos. Antiviral Research 76, 1-10 (2007). [ PubMed ] [ Google Acadêmico ]
- 22. Riehle P., Rusche N., Saake B. & Rohn S. Influência do conteúdo foliar e tamanho das partículas de ervas na presença e extração de compostos fenólicos foram quantificados em chás de ervas Cistus incanus . Journal of Agricultural and Food Chemistry 62, 10.978-10.988 (2014). [ PubMed ] [ Google Acadêmico ]
- 23. Barrajón-Catalán E. et al. Estudo sistemático da composição polifenólica de extratos aquosos derivados de várias espécies do gênero Cistus: relação evolutiva. Phytochemical Analysis 22, 303-312 (2011). [ PubMed ] [ Google Acadêmico ]
- 24. Daglia M. Polyphenols como agentes antimicrobianos. Opinião Atual em Biotecnologia 23, 174-181 (2012). [ PubMed ] [ Google Acadêmico ]
- 25. Andrae-Marobela K., Ghislain FW, Okatch H. & Majinda RR polifenóis: uma classe diversificada de agentes anti-HIV-1 multiobjetivos. O metabolismo atual de drogas 14, 392-413 (2013). [ PubMed ] [ Google Acadêmico ]
- 26. Ehrhardt C. et al. Um extrato de polifenol rico em plantas, CYSTUS052, exerce atividade contra o vírus influenza na cultura celular sem efeitos colaterais tóxicos ou tendência a induzir resistência viral. Antiviral Research 76, 38-47 (2007). [ PubMed ] [ Google Acadêmico ]
- 27. Kalus U., Kiesewetter H. & Radtke H. Efeito do CYSTUS052® e chá verde sobre sintomas subjetivos em pacientes com infecção do trato respiratório superior. Pesquisa em fitoterapia 24, 96-100 (2010). [ PubMed ] [ Google Acadêmico ]
- 28. Kalus U. et al. Incanus Cistus (CYSTUS052) para o tratamento de pacientes com infecção do trato respiratório superior: um estudo clínico prospectivo, randomizado e controlado por placebo. Antiviral Research 84, 267-271 (2009). [ PubMed ] [ Google Acadêmico ]
Esta ficha é apenas informativa, não dispensando o conselho do seu médico ou técnico de saúde.
Todas as pessoas antes de tomarem um produto natural devem informar-se de que o mesmo está em consonância com o seu padrão genético (grupo sanguíneo) e, na dúvida, não tomem pois correm o risco de gastarem dinheiro e, pior que tudo, estarem a adoecer em vez de prevenirem ou tratarem.


 Lindsay é bacharel em ciências biomédicas, com ênfase em nutrição, pela Universidade Nacional de Ciências da Saúde. Quando não está estudando nutrição ou pesquisando e escrevendo, Lindsay gosta de malhar, escalar montanhas, fazer caminhadas, esquiar e se aventurar ao ar livre. Ela também é bastante apaixonada por sua câmera e por tirar fotos da natureza. Você pode ler mais sobre a experiência da doença de Lyme de Lindsay, bem como ler todos os seus pensamentos e pesquisas mais recentes sobre saúde, visitando seu blog,
Lindsay é bacharel em ciências biomédicas, com ênfase em nutrição, pela Universidade Nacional de Ciências da Saúde. Quando não está estudando nutrição ou pesquisando e escrevendo, Lindsay gosta de malhar, escalar montanhas, fazer caminhadas, esquiar e se aventurar ao ar livre. Ela também é bastante apaixonada por sua câmera e por tirar fotos da natureza. Você pode ler mais sobre a experiência da doença de Lyme de Lindsay, bem como ler todos os seus pensamentos e pesquisas mais recentes sobre saúde, visitando seu blog, 

 Potente actividade antiviral contra o Vírus Influenza humano e aviário:
Potente actividade antiviral contra o Vírus Influenza humano e aviário: Cistus Incanus vs Placebo no tratamento de infecções respiratórias superiores. Maior diminuição de sintomas nos pacientes tratados com Cistus Incanus. A proteína C-reactiva (marcador inflamatório) diminuiu significativamente nos pacientes que receberam o tratamento:
Cistus Incanus vs Placebo no tratamento de infecções respiratórias superiores. Maior diminuição de sintomas nos pacientes tratados com Cistus Incanus. A proteína C-reactiva (marcador inflamatório) diminuiu significativamente nos pacientes que receberam o tratamento: Cistus Incanus ( la jara em espanhol) na doença de Lyme e em fumadores:
Cistus Incanus ( la jara em espanhol) na doença de Lyme e em fumadores: Artigo sobre a Cistus em infecções respiratórias e pele:
Artigo sobre a Cistus em infecções respiratórias e pele:
 Benefícios das Cistus no tratamento da Hipertrofia Benigna da Próstata:
Benefícios das Cistus no tratamento da Hipertrofia Benigna da Próstata: Dr. Dietrich Klinghardt aconselha Cistus Incanus na doença de Lyme :
Dr. Dietrich Klinghardt aconselha Cistus Incanus na doença de Lyme :
 DENTES Mais Brancos
DENTES Mais Brancos







